浅野中学2011年の問題。
次の[実験1]と[実験2]をもとに、後の(1)~(6)の問いに答えなさい。
ただし、実験に使うステンレス皿は反応しないものとします。
[実験1]
26.6gのステンレス皿に銅の粉末を入れ、上皿天秤で全体の重さを測りました。次に、ステンレス皿を三脚の上にのせて、ガスバーナーで加熱すると、銅の粉末は空気中の気体Aと反応して、固体物質Bになりました。その後で再び、上皿天秤で全体の重さを測りました。
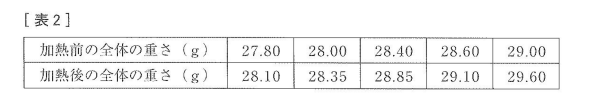
この実験を鋼の粉末の重さを変えて行った結果、[表2]のようになりました。
[実験2]
[実験1]とは違う重さのステンレス皿に固体物質Cを入れ、上皿天秤で全体の重さを測りました。次に、ステンレス皿を三脚の上にのせて加熱すると、固体物質Cは銀と気体Aに容易に分解しました。気体Aを水素と完全に反応させると、気体Dが生じました。気体Dを冷やして完全に液体にしてから、液体Dの重さを測りました。
この実験を固体物質Cの重さを変えて行った結果、[表3]のようになりました。

(1〕気体Aと液体Dの名前を答えなさい。
(2)次のア~オの実験のうち、気体Aが発生するのはどれですか。正しいものを1つ選び、その記号で答えなさい。
ア 石灰石に塩酸を加える。
イ 鉄くぎに硫酸を加える。
ウ 重曹(炭酸水素ナトリウム)を加熱する。
エ 二酸化マンガンに過酸化水素水を加える。
オ アルミニウムに水酸化ナトリウム水溶液を加える。
(3)固体物質Bができるとき、反応する銅と気体Aの重さの比を、もっとも簡単な整数比で答えなさい。
(4)[表3]のX、Yに入る数値を答えなさい。
(5)[実験2]で用いたステンレス皿の重さは何gですか。
(6)液体Dができるとき、反応する気体Aと水素の重さの比を、もっとも簡単な整数比で答えなさい。
さらっと酸化銀が出てきているので、これはやはり研究しておきましょう。
子どもたちが普通ならうのは加熱して酸化させる方法。銅→酸化銅はこうやって作ります。したがって実験1はわかりやすい。
ただ表2はデータの処理をしないといけません。皿が26.6gあるからそれぞれ引くと次のような表が出来上がります。
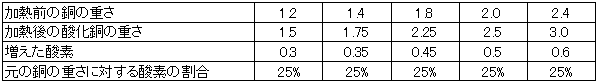
ということで銅と酸素が4:1の重さで結びついていることがわかります。ここまでは理解しやすい話でしょう。
この逆の反応を熱を与えて行っているのが実験2です。酸化と還元の話になってきています。
酸化→酸素を付ける
還元→酸素を取り除く
と考えてください。酸化銅の場合、還元させるには銅とくっついている酸素をほかの物資にくっつけることで、銅から引き離します。
これが還元剤で、例えば水素や炭素を入れて酸素を取り除くのです。
炭素を入れて加熱すると、酸素は炭素を化合して二酸化炭素になります。その結果として黒かった酸化銅は赤みを帯びて、銅にもどることになります。もし水素を送りながら加熱すれば、酸素は水素と結びついて水となり酸素が取り除かれるというしくみです。
ところが酸化銀は加熱するだけで、銀と酸素が分離します。くっついている酸素を別のものにくっつけなくても、酸素と銀が分かれるのです。
これを知っている必要があるか? ということになると基本的には知らなくてもいいでしょう。
この問題の冒頭に酸化銅の話が出てきているので、これは銀と酸素が結びついているものが固体Cだとわかってくれれば良い。
気体Aは実験1でも出てきていますので、Aは酸素だということはわかります。それが銀と結びついていたのだから、物質Cは酸化銀だろう、ということがわかればいいのですから。
酸素と水素が結びつけば水ですから気体Dは水蒸気になり、液体Dは水ということになるでしょう。
(1)(答え)気体A 酸素 液体D 水
(2)酸素を発生させる実験です。 (答え)エ
(3)上の表からわかります。(答え)4:1
(4)表3から考えます。
一番左の項目で、加熱前の全体の重さは46.2g 加熱後の重さは45.4g
この差は46.2-45.4=0.8gでこれが酸素です。
一方水は0.9gできていますから、0.1gの水素と結びついたことがわかります。
次の項目の加熱後の重さである55.4gはその左の45.4gに比べて何が増えているか?というと銀だけです。では、銀はいったいどのくらいの割合で酸素と結びついているのかを調べましょう。
1項目目と3項目目の差に注目します。
78.6-46.2=32.4 酸化銀の増加
75.4-45.4=30 銀の増加
だから、酸素の重さは2.4g増加しているので 30:2.4=150:12=25:2の重さの比で銀と酸素が結びついています。
2項目へは1項目目に比べて銀の重さが10g増えているので、この分の酸化銀は
10×27/25=10.8g
したがってX=46.2+10.8=57g とわかります。
加熱後減少した酸素は57-55.4=1.6gだから 減少した酸素:水=8:9より
1.6×9/8=1.8g
(4)(答え)X 57g Y 1.8g
そうすると最初の項目で、減少した酸素が0.8gですから、酸化銀は0.8×27/2=10.8g あったことがわかるので、
46.2-10.8=35.4gが皿の重さです。
(5)(答え)35.4g
(6)酸素が0.8gのときに水が0.9g 水素は0.1gになります。
(答え)8:1
なかなか難しい問題かもしれません。男子受験校らしい出題と言えるでしょう。
==============================================================
中学受験で子どもと普通に幸せになる方法、本日の記事は
夏の合宿って意味があるの?
==============================================================
今日の慶應義塾進学情報
はやくも
==============================================================









